
![]()
(c
 |
)
|
Gyvsidabris |
||||
|
|
||||
 |
||||
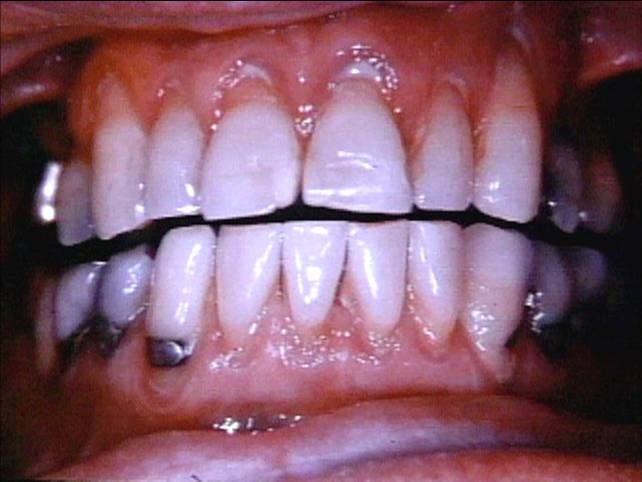
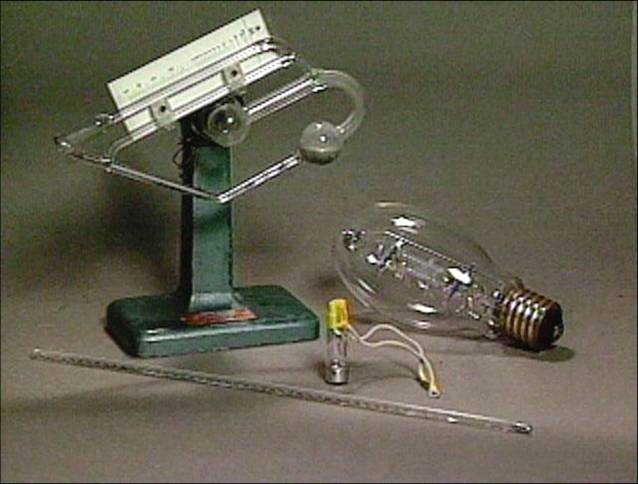
| Naudojimas: dantų plombų gamyboje ( Ag-Sn amalgamos), termometruose, manometruose, barometruose, dienos šviesos lempose, kvarco lempose. | ||||
 |
 |
|||
| Sąveika su oro deguonimi | ||||
|
2Hg (s) + O2 (d) → 2HgO (s) |
||||
 |
||||
| Sąveika su rūgštimis | ||||
|
Gyvsidabris reaguoja su azoto
rūgštimis: 6Hg (s) + 8HNO3 (prask.) → 3Hg2(NO3)2 (aq) + 2NO (d) +4H2O (s) Hg (s) + 4HNO3 (konc.) → Hg2(NO3)2 (aq) + 2NO2 (d) +2H2O (s) |
||||
 |
 |
 |
||
| Gyvsidabrio (II) jodido susidarymo termodinaminis reguliavimas | ||||
|
Į kairėje esančią
stiklinę su Hg 2+(II) jonais įpilama tirpalo,
turinčio nedidelę I- jonų koncentraciją, o į dešinėje
esančią – didelę koncentraciją. Kairiojoje stiklinėje tirpalas akimirksniu tampa geltonas, po to ryškiai oranžinis. Dešiniojoje per tą patį laiką - tik geltonas. Geltona spalva rodo, kad susidaro rombinę gardelę turintis HgI2. Oranžinė spalva – tetragoninė gardelė.
|
||||
 |
 |
 |
||
 |
 |
 |
||
 |
|
|||
Vienintelis visų teisių savininkas (įskaitant visas su juo
susijusias autorines teises) į
Chemistry Comes Alive!
vaizdinę – foto medžiagą yra
Journal of Chemical Education.
Visos teisės saugomos. Naudojama turint leidimą.




