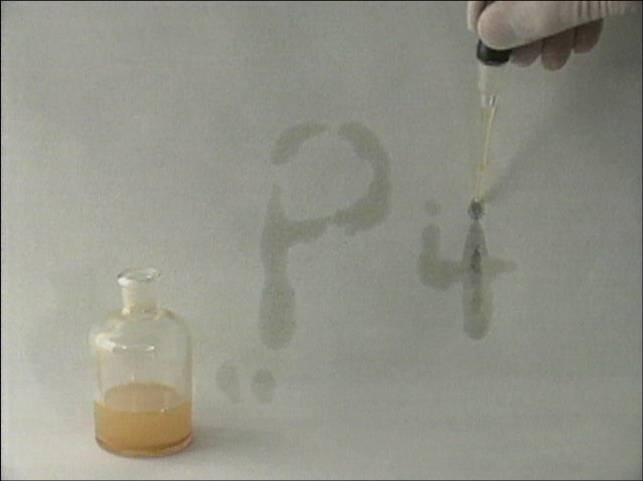| |
Sąveika su oro deguonimi
( balto fosforo "rašalas")
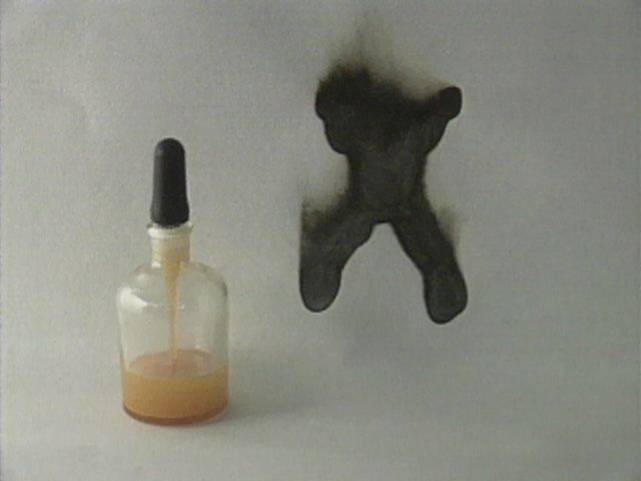
Balto fosforo, ištirpinto anglies disulfide, įtraukiama medicinine
pipete ir lašinama ant filtravimo popieriaus. Blyškiai geltonos spalvos
balto fosforo užrašas gerai matomas. Anglies disulfidas išgaruoja ir
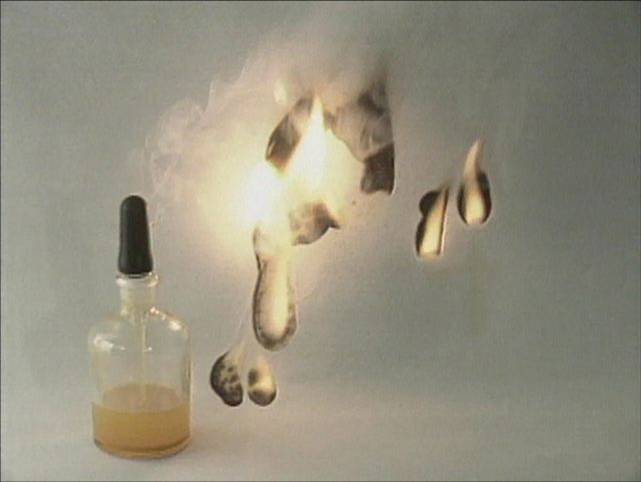
fosforas pradeda reaguoti su oro deguonimi –užsidega.
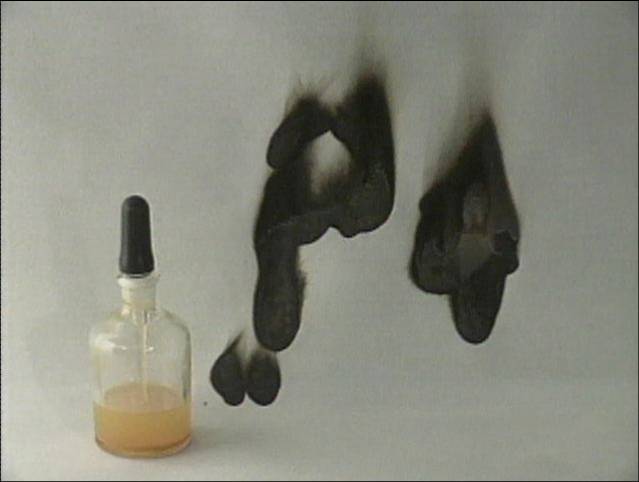
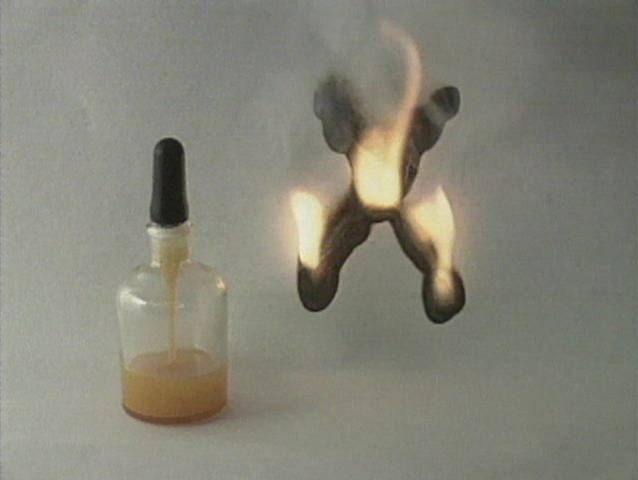
Degimas - egzoterminė reakcija, kurios metu popieriaus dalis, ant kurios yra
balto fosforo “rašalas”, sudega:
P4 (k) + O2 (d)
→ P4O10
(k)
Balto fosforo molekulė P4 – tetraedrinės struktūros molekulė. Tamsoje
fosforas šviečia žalia spalva. Drėgname ore baltas fosforas savaime užsidega
esant 30º C. Sausame ore užsidega esant aukštesnei temperatūrai. Baltas
fosforas labai nuodingas, daug nuodingesnis nei kitos juodos ar raudonos jo
alotropinės atmainos.
|
|

![]()