
![]()
(c
 |
)
|
HCl (aq) elektrolizė |
||||
| Elektrolizės bandymams atlikti galima panaudoti labai paprastą prietaisą | ||||
|
|
|
|||
| Į viršų | ||||
| HCl (aq) elektrolizė | ||||
|
Redukcija prie
katodo:
2H+ (aq) + 2e- → H2 (d) Oksidacija prie anodo: 2H2O (s) → 4H+(aq) + O2 (d) + 4e- |
||||
 |
 |
|||
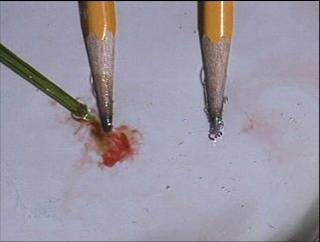
| Įpylus indikatoriaus prie anodo ir katodo, jo spalva parodė, kad terpė prie abiejų elektrodų yra rūgštinė | ||||
 |
 |
|||
|
Į viršų |
||||
| NaOH (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O (s) + 2e-
→ H2 (d) + 2OH-
(aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
| Įpylus indikatoriaus prie anodo ir katodo, jo spalva parodė, kad terpė prie abiejų elektrodų yra bazinė | ||||
 |
||||
|
Į viršų |
||||
| NaCl (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O (s) + 2e-
→ H2 (d) + 2OH-
(aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
| Įpilus indikatoriaus prie anodo, jo spalva parodė, kad terpė yra rūgštinė, o prie katodo - bazinė | ||||
|
|
||||
 |
 |
|||
|
Į viršų |
||||
| Distiliuotas vanduo | ||||
| Distiliuotos vandens tirpalas elektros srovės nepraleidžia, elektrolizė nevyksta | ||||
 |
 |
|||
|
Į viršų |
||||
| SnCl4 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
Sn4+ (aq)
+ 2e- → Sn2+
(k) ir 2H2O (s) + 2e-
→ H2 (d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| SnCl2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
Sn2+
(aq) + 2e- → Sn (k)
Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| NaNO3 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Mg(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d.) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Al(NO3)3 (aq) elektrolizė | ||||
|
Redukcija prie katodo: 2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| KNO3 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Ca(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Co(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
Co2+
(aq) + 2e- → Co (k)
ir
2H2O (s) + 2e-
→ H2 (d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Ni(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo: Ni2+
(aq) + 2e- → Ni
(k) ir
2H2O (s) + 2e-
→ H2 (d) + 2OH-
(aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
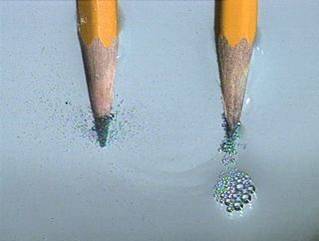 |
|||
|
Į viršų |
||||
| Cu(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
Cu2+
(aq) + 2e- → Cu (k)
ir 2H2O (s) + 2e-
→ H2 (d) + 2OH-
(aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Zn(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo: Zn2+
(aq) + 2e- → Zn (k)
Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e |
||||
 |
 |
|||
|
Į viršų |
||||
| Cr(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo: 2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| AgNO3 (aq) elektrolizė | ||||
|
Redukcija prie katodo: Ag+
(aq) + e- → Ag (k)
Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Ba(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
2H2O
(s) + 2e- → H2
(d) + 2OH- (aq) Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
|
Į viršų |
||||
| Pb(NO3)2 (aq) elektrolizė | ||||
|
Redukcija prie katodo:
Pb2+
(aq) + 2e- → Pb (k)
Oksidacija prie anodo: 4OH- (aq) → 2H2O (s) + O2 (d) + 4e- |
||||
 |
 |
|||
| Į viršų | ||||
Vienintelis visų teisių savininkas (įskaitant visas su juo
susijusias autorines teises) į
Chemistry Comes Alive!
vaizdinę – foto medžiagą yra
Journal of Chemical Education.
Visos teisės saugomos. Naudojama turint leidimą.




